tema
Rene
I reni e le vie urinarie sono posti nella zona retroperitoneale, a diretto contatto con il peritoneo. Il rene destro e ribassato di circa 2-3 cm rispetto a quello di sinistra. Posteriormente i reni sono protetti dalla massa muscolare dorsalementre lateralmente sono difessi dalle ultime costole. Il parenchima renale ha la funzione di filtrare il sangue per produrre l’urina. Menttre i calici renali, il bacinetto renale, l’uretere, la vescica e l’uretere hanno funzione di trasporto, accumulo ed espulsione dell’urina.
Per capire in pieno le patolgie malformative renali e’ indispensabile comprendere l’embriologia dell’apparato genitourinario.
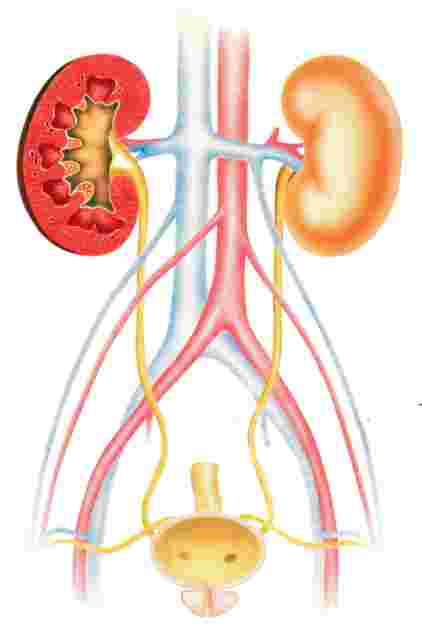
Agenesia Renale
L’agenesia renale bilaterale è una condizione estremamente rara, con circa 500 casi descritti in letteratura. Questa malformazione è incompatibile con la vita, poiché causa morte prenatale o entro le prime 48 ore dalla nascita, a causa di una grave insufficienza respiratoria attribuibile alla presenza di oligoidramnios.
L’agenesia renale unilaterale si osserva invece ogni 1000-1500 nascite ed è più frequente nei maschi. Se l’arresto dello sviluppo avviene prima della quarta settimana di gestazione, può associarsi a un’agenesia completa dell’apparato genitale omolaterale. Nella maggior parte dei casi, la gonade, originata dalla plica genitale vicina al pronefro, si sviluppa normalmente; tuttavia, le strutture derivate dai dotti di Wolff e di Muller possono essere assenti, rudimentali o comunque anomale: questo può riguardare l’epididimo, il dotto deferente, le vescicole seminali, le tube e la vagina.
Al contrario, difetti di involuzione di queste strutture portano a condizioni più rare e clinicamente poco rilevanti, come le cisti del dotto di Gartner nelle femmine e l’organo di Giraldès nei maschi. In genere, l’agenesia renale unilaterale non provoca sintomi clinici, e la sua scoperta è spesso casuale. La diagnosi viene effettuata tramite ecografia o urografia. La TAC può essere necessaria per distinguere l’agenesia da una ipoplasia renale in sede ectopica, e permette inoltre di rilevare malformazioni genitali associate, particolarmente nelle donne (ad esempio, utero unicorne, utero didelfo, atresia vaginale, ecc.).
Una caratteristica distintiva dell’agenesia renale è l’assenza della via escretrice: pertanto, la cistoscopia può mostrare l’assenza o l’ipoplasia dell’emitrigono e dell’orifizio ureterale. La prognosi per questi pazienti non è generalmente compromessa, poiché il rene controlaterale non è maggiormente suscettibile a malattie nonostante la sua unicità.
Displasia renale e malattia cistica
La displasia renale è una condizione rara e di difficile inquadramento patogenetico, rappresentando un’espressione di deficit evolutivo della gemma nefrogena. Pur essendo in linea con l’agenesia renale, in realtà presenta abbozzi vestigiali della gemma nefrogena, costantemente presenti in diversa misura. La diagnosi in età pediatrica è spesso facilitata dalla frequente associazione con altre malformazioni o da sintomi di compressione e dislocazione di organi contigui, dovuti all’aumento volumetrico.
I disturbi urinari veri e propri sono rari; specialmente nelle forme che si diagnosticano nell’adulto, la diagnosi è spesso casuale. Il rene si presenta costituito da grosse cavità cistiche a parete fibrosa, calcificata tipicamente a “guscio d’uovo”, contenente liquido giallastro. Non si osservano strutture vasali macroscopicamente evidenti e l’uretere prossimale è atresico.
Istologicamente, all’ilo si può avere un ammasso di tessuto fibroso in cui si riscontrano ammassi di strutture tubulari di vario calibro e forma. La diagnosi si basava sulla triade radiologica di Kjaw: silenzio funzionale del rene e calcificazioni a guscio d’uovo all’urografia, atresia dell’uretere prossimale all’ureterografia retrograda e ipoplasia dell’arteria renale all’angiografia. Oggi la diagnosi avviene tramite ecografia e TAC, che permettono di identificare gli elementi caratteristici di questa malformazione.
La possibilità di una diagnosi ragionevolmente accurata non esime dall’indicazione all’esplorazione chirurgica e alla conseguente exeresi: la profonda indifferenziazione e dedifferenziazione di queste strutture vestigiali contiene in sé tanto potenziale oncogeno da sollevare dubbi sull’innocuità attuale o potenziale di questa malformazione (Gutter; Potenzoni et al.).
Una forma particolare di displasia è il rene cistico multiloculare (RCM), che deriva da anomalie di sviluppo globale del blastema metanefrico. La differenza rispetto alla malattia cistica renale più tipica risiede nell’assenza di parenchima renale maturo nei setti intercistici, costituiti invece da connettivo fibrillare e fibroso, fasci di muscolatura liscia e strutture vascolari immature. In alcune osservazioni in infanzia, la presenza di microfocolai di nefroblastoma ha suggerito una comune origine tra il tumore di Wilms e il rene cistico multiloculare.
Con criteri quantitativi, si sono proposti i termini (IOSHI et al., 1989) di nefroblastoma cistico parzialmente differenziato (elementi singoli, disseminati, di blastema immaturo) e di rene cistico multiloculare con noduli di tumore di Wilms. Sono stati descritti anche pochi casi di associazione tra rene cistico multiloculare e carcinoma a cellule renali, considerata casuale poiché il carcinoma a cellule renali origina da porzioni di nefrone maturo che, per definizione, non si sviluppano nella displasia multicistica. Tuttavia, l’associazione fortuita, senza corresponsabilità patogenetiche, è possibile nel caso di rene cistico multiloculare segmentario.
Su queste osservazioni, e sull’osservazione di effettive trasformazioni maligne, solitamente di natura connettivale, si basa l’alternativa teoria patogenetica neoplastica del rene cistico multiloculare. Sono frequenti le associazioni di rene cistico multiloculare con altre malformazioni urinarie ed extraurinarie, spesso prevalenti sul piano clinico. Il rene cistico multiloculare non è una condizione ereditabile; è più spesso monolaterale, con una preferenza per il lato sinistro. Le forme bilaterali sono rare e spesso incompatibili con la vita, così come le forme segmentarie.
Questa condizione può manifestarsi clinicamente in tutte le età, ma specialmente nella quinta e settima decade. Le femmine sono più colpite dei maschi, con un rapporto di circa 2 a 1. I problemi clinici includono: insufficienza renale, correlata all’estensione della displasia (bi- o monolaterale; totirenale o segmentaria); disturbi da occupazione di spazio retroperitoneale; ematuria e/o ipertensione, ovviamente in relazione alla persistenza di una via escretrice pervia e con la presenza di parenchima maturo nelle forme segmentarie.
I sintomi e segni iniziali, in ordine di frequenza, sono: massa palpabile o rilevata da ecografia occasionale (47%), dolore addomino-lombare (34.5%), ematuria (25%), e ipertensione (14-15%). Le calcificazioni periferiche ai raggi, agli ultrasuoni e alla TAC, insieme alla deformazione del profilo renale e all’identificazione dei setti intercistici, meno densi del tessuto normale e privi di “enhancement” all’angio TAC, consentono un orientamento diagnostico differenziale nei confronti del rene policistico, non sempre chiaramente differenziabile dal tumore renale necrotizzato (specie nelle forme segmentarie).
Per questo motivo, e per la possibilità teorica della trasformazione da displasia multicistica a neoplasia, è consigliato un follow-up serrato e un tempestivo intervento diagnostico exeretico, con eventuali intenti conservativi (nelle forme segmentarie?), oggi da prendere in considerazione anche nei confronti delle neoplasie conclamate.
Il rene policistico
È una malformazione non rara (1/250-1/100) di tipo ereditaria, con carattere sia autosomico recessivo (che si evidenzia più frequentemente alla nascita o nell’età infantile) sia autosomico dominante (che si evidenzia più frequentemente in età adulta). Questa condizione consiste in numerosi ammassi di cisti permeanti il parenchima renale normale, che viene a costituire un traliccio intercistico, distorto, stirato e compresso, insieme con la via escretrice intrarenale.
La malformazione è bilaterale, anche se può presentare una notevole asimmetria di evoluzione anatomopatologica. Ha una distribuzione uguale tra i due sessi. La teoria patogenetica si basa sulla persistenza di tubuli uriniferi primitivi (2ª-4ª generazione), per difetto di atrofia, in eccesso rispetto alle suddivisioni terminali della gemma ureterogena wolffiana.
Accanto al meccanismo di dilatazione progressiva passiva del nefrone prossimale, se cernente e non defluente (teoria meccanica di CARONE et al., 1974), si affianca la più moderna ipotesi del ruolo attivo della membrana basale dell’epitelio nefronale, stimolata dall’intervento della matrice mesenchimale extracellulare in situazioni solo ipotizzabili, infettive, biochimiche, ecc. Lo stesso meccanismo, valido anche per la cisti semplice, sembra trovare riscontro in esempi di malattia cistica acquisita, come in condizioni di insufficienza renale cronica (dializzati) oppure di ipopotassiemia cronica.
Secondo questa teoria e secondo riscontri sperimentali, si formano prima dei cordoni o masse solide da iperplasia epiteliale, che secondariamente si cavitano. Si inscrive razionalmente, nel concetto di epitelio cistico “attivo”, la possibilità della trasformazione maligna dell’iperproliferazione epiteliale: cisti-cancro.
La malattia cistica si manifesta clinicamente, specialmente per l’occupazione di spazio nei confronti del parenchima normale, a contatto con lo spazio retroperitoneale e addominale, nonché con il progressivo deterioramento della funzione renale e i sintomi delle complicanze infettive. Il rene policistico può essere così sviluppato alla nascita da causare distocia e condurre a morte entro pochi mesi.
In più della metà dei casi, il decorso è graduale e si manifesta dopo i 25-30 anni di vita. La diagnosi viene effettuata tramite palpazione, ecografia, radiologia, TAC, angio-TC e nefroscan, consentendo di differenziare da tumori, rene multiloculare e idronefrosi.
Una caratteristica costante e patognomonica è l’aumento volumetrico del rene in toto, specie in lunghezza (superiore a un tratto trivertebrale di rachide). L’evacuazione di cisti voluminose e/o infette, oggi ecoguidate a cielo coperto, può procrastinare l’insufficienza renale e la necessità di exeresi.
Anomalie di sede e di rotazione
Quando il tronco fetale si raddrizza e si allunga in senso caudale, il rene sembra risalire nella cavità addominale fino alla sua sede lombare definitiva. Tuttavia, una diminuzione del potere evolutivo intrinseco della massa metanefrogenica può rallentare lo sviluppo della gemma ureterale, determinando una discrepanza tra la velocità di sviluppo del sistema urinario e l’allungamento del tronco. Sono state ipotizzate anche la mancata involuzione di strutture vascolari a connessione sacrale.
L’ectopia renale va distinta dalla ptosi renale, condizione nella quale il rene si disloca dalla posizione normale in certe posizioni e movimenti, pur mantenendo connessioni vascolari in sede normale. L’ectopia può essere:
- Semplice: quando il rene si trova in posizione anomala, pur restando dallo stesso lato.
- Crociata: quando il rene migra al lato controlaterale.
L’incidenza dell’ectopia semplice è di 1/900 nati e viene classificata in base alla posizione:
- Pelvica: il rene è situato di fronte al sacro e al di sotto della biforcazione aortica.
- Iliaca: il rene è adagiato sul promontorio sacrale vicino ai vasi iliaci.
- Lombare basso: adiacente alla 2ª vertebra lombare.
- Toracico: molto raramente situato al di sopra della parete postero-laterale del diaframma (forame di Bockdalek).
Spesso (15-45%), l’ectopia si associa a anomalie genitali, mentre solo raramente le ghiandole surrenali sono assenti o in sede anomala. La maggior parte dei reni ectopici è asintomatica, e la scoperta è quindi del tutto casuale; altrimenti, possono manifestarsi con infezioni o dolori addominali che, in tal caso, non presenteranno le caratteristiche tipiche della colica renale, portando a diagnosi errate (appendicite, annessite, ecc.).
Il rene ectopico può essere suscettibile a idronefrosi e conseguente calcolosi, a causa della malrotazione del rene e della disposizione anteriore della pelvi, nonché per l’anomala vascolarizzazione; inoltre, comporta una maggiore esposizione ai traumi addominali.
La diagnosi viene effettuata tramite esame urografico; tuttavia, un rene ectopico ipoplasico situato davanti al sacro può essere mascherato e di difficile diagnosi. La Risonanza Magnetica o la TC permettono un’agevole diagnosi della massa pelvica e di anomalie genitali associate. L’arteriografia può essere indicata solo nel caso di intervento chirurgico, per identificare la vascolarizzazione anarchica del rene (presenza di 2-3 arterie renali a partenza dalle iliache o dalla parte caudale dell’aorta).
Nell’ectopia crociata, il rene si trova nel lato opposto rispetto a quello in cui il proprio uretere si inserisce nella vescica. Il rene ectopico si trova più frequentemente al di sotto del rene normale, con il quale, nel 90% dei casi, presenta anche una fusione parenchimale. Questa condizione è rara, prevalente nei maschi e generalmente il rene sinistro migra verso il lato destro.
Gli aspetti clinici non si discostano da quelli descritti per l’ectopia semplice, e la diagnosi si fa esclusivamente con la visualizzazione della via escretrice (urografia, pielografia ascendente). La terapia è richiesta solo in caso di complicanze.
Anomalie di fusione
Un difetto di separazione della struttura metanefrogenica provoca la fusione delle due strutture renali, ognuna con il proprio apparato escretore, che rimangono comunicanti a livello parenchimale. Queste strutture presentano:
- Vascolarizzazione anomala di tipo fetale
- Incompleta rotazione, per cui i due bacinetti renali si troveranno in posizione mediale-anteriore.
Si possono osservare varie forme di fusione, tra cui:
- Fusione del polo inferiore di un rene con il polo superiore dell’altro (“rene ad elle” o “esse”).
- Fusione di tutti e quattro i poli (“rene a focaccia”).
- La forma più comune è l’unione dei due poli inferiori, che determina il “rene a ferro di cavallo”.
In quest’ultimo caso, i poli inferiori dei reni si presentano uniti da un istmo, che può essere fibroso o parenchimale. Questa condizione è stata riscontrata nello 0,25% della popolazione e colpisce con una incidenza doppia i maschi. L’istmo è situato al di sotto dell’arteria mesenterica inferiore, che ne blocca l’ulteriore risalita.
La vascolarizzazione del rene è estremamente variabile, e solo nel 30% dei casi è fornita da una sola arteria renale per ogni rene. I calici sono orientati in modo atipico, con quelli inferiori disposti orizzontalmente per drenare il ponte. Il bacinetto è situato anteriormente, e i due ureteri scavalcano l’istmo.
Il rene a ferro di cavallo è spesso associato a altre anomalie, in particolare dello scheletro, dell’apparato cardiovascolare e genitale. Un terzo dei pazienti rimane asintomatico, mentre negli altri casi la malformazione facilita complicanze legate a:
- Difficoltà del drenaggio escretorio
- Problemi di irrorazione
Queste complicanze includono idronefrosi, calcolosi e infezione, con sintomi correlati come sepsi, dolore, ematuria e piuria. Un’ostruzione della giunzione pieloureterale è presente nel 30% dei casi, e la calcolosi varia dal 20 all’80%.
La diagnosi viene effettuata nella quasi totalità dei casi tramite urografia, che dimostra:
- Abbassamento delle immagini renali
- Anteriorizzazione del bacinetto
- Poli inferiori e calici intrapontini indefinibili o sfumati
- Variazione degli assi longitudinali dei reni, che convergono verso il basso
La scintigrafia renale visualizzerà la fusione dei poli inferiori e la presenza di un istmo parenchimale o fibroso.
Il trattamento del rene a ferro di cavallo è correlato esclusivamente all’insorgenza delle complicanze, che quasi sempre richiedono un intervento chirurgico. L’idronefrosi è spesso collegata a una disectasia giuntale concomitante e deve essere trattata con una resezione e plastica del giunto.
Nell’ipotesi che l’idronefrosi sia imputabile alla compressione esercitata sull’uretere che scavalca il ponte, si può ricorrere a una separazione dei due reni mediante sinfisiotomia. Tuttavia, il beneficio della divisione dell’istmo nei confronti del dolore e dell’idronefrosi è ottenuto raramente, limitando l’economicità dell’intervento, che presenta rischi, specialmente se il ponte contiene parenchima renale o un calice intrapontinico.
In taluni casi, l’atrofia idronefrotica di un emirene può comportare l’asportazione del parenchima e delle sue strutture escretrici. Questo intervento è comunque difficile da eseguire e può rendere necessaria una visualizzazione preoperatoria mediante arteriografia, quasi sempre anomala.
Bibliografia
- Walsh P.C., Retik A.B., Stamey T.A., Vaughan E.D.: Urologia di Campbell, 2\’b0 edizione italiana tradotta dalla 6\’b0 edizione americana, 1993 Verducci Editore;
- Bezzi E.: Urologia, 1974 UTET, Torino
- Ashcraft K.W.: Pediatric Urology, 1990 W.B. Saunders Company;
- Libertino J.A.: Pediatric and adult reconsctructive urologic surgery, 1987 2 edition, Williams & Wilkins;
- Tanagho E.A., McAminch J.W.: Smith’s General Urology, 1988 twelfth edition, Appleton & Lange